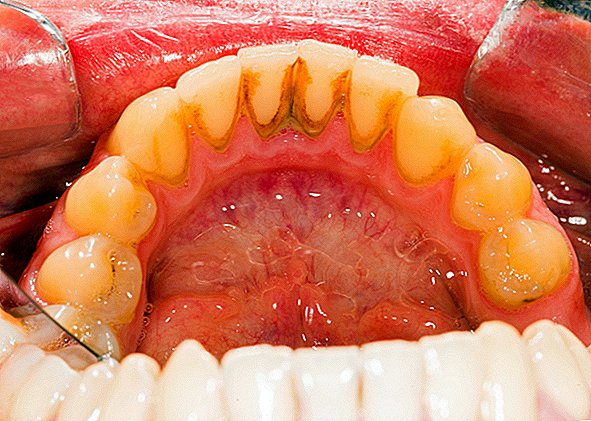
Biofilmi su skup jedne ili više vrsta mikroorganizama koji mogu rasti na različitim površinama. Mikroorganizmi koji tvore biofilme uključuju bakterije, gljivice i protiste.
Jedan čest primjer zubnog plaka na biofilmu, gnojna nakupina bakterija koja se formira na površinama zuba. Ribnjak ribnjaka je još jedan primjer. Otkriveni su biofilmi na mineralima i metalima. Pronađeni su pod vodom, pod zemljom i iznad zemlje. Oni mogu rasti na biljnim tkivima i životinjskim tkivima, te na implantiranim medicinskim uređajima poput katetera i pejsmejkera.
Svaka od ovih karakterističnih površina ima zajedničko svojstvo: mokro je. Ta se okruženja "povremeno ili kontinuirano gube vodom", navodi se u članku iz 2007. objavljenom u časopisu Microbe Magazine. Biofilmi uspevaju na vlažnim ili vlažnim površinama.
Biofilmi su se već dugo vremena etablirali u takvim okruženjima. Fosilni dokazi biofilma datiraju prije otprilike 3,25 milijardi godina, navodi se u članku iz 2004. objavljenom u časopisu Nature Reviews Microbiology. Primjerice, biofilmi su pronađeni u 3,2 milijarde godina dubokim morskim hidrotermalnim stijenama kratona Pilbara u Australiji. Slični biofilmi nalaze se u hidrotermalnim okruženjima poput vrućih izvora i otvorenih otvorenih mora.

Formiranje biofilma
Formiranje biofilma započinje kada mikroorganizmi koji slobodno plutaju, poput bakterija, dođu u kontakt s odgovarajućom površinom i počnu ostavljati korijenje, tako reći. Prvi korak povezivanja događa se kada mikroorganizmi proizvode gnojnu tvar poznatu kao vanćelijska polimerna tvar (EPS), prema Centru za biofilm inženjering na Sveučilištu Montana. EPS je mreža šećera, proteina i nukleinskih kiselina (poput DNK). Omogućuje da se mikroorganizmi u biofilmu sjedine.
Nakon vezanosti slijedi razdoblje rasta. Daljnji slojevi mikroorganizama i EPS nadograđuju se na prvim slojevima. Konačno, oni stvaraju žarnu i složenu 3D strukturu, prema Centru za biofilm inženjering. Vodeni kanali križaju biofilmove i omogućavaju razmjenu hranjivih i otpadnih proizvoda, navodi se u članku iz Microbe.
Višestruki okolišni uvjeti pomažu odrediti u kojoj mjeri biofilm raste. Ti čimbenici također određuju je li sačinjena od samo nekoliko slojeva stanica ili značajno više. "To stvarno ovisi o biofilmu", rekao je Robin Gerlach, profesor na katedri za kemijsko i biološko inženjerstvo na Državnom sveučilištu Montana-Bozeman. Na primjer, mikroorganizmi koji stvaraju veliku količinu EPS-a mogu prerasti u prilično guste biofilmove čak i ako nemaju pristup puno hranjivih sastojaka, rekao je. S druge strane, za mikroorganizme koji ovise o kisiku, raspoloživa količina može ograničiti njihov porast. Drugi čimbenik okoliša je koncept "posmičnog naprezanja". "Ako imate vrlo velik protok kroz biofilm, poput potoka, biofilm je obično prilično tanki. Ako imate biofilm u vodi koja sporo teče, poput ribnjaka, može postati vrlo gust", objasnio je Gerlach.
Napokon, stanice unutar biofilma mogu napustiti nabor i uspostaviti se na novoj površini. Ili se nakupina stanica odvoji, ili se pojedine stanice razbiju iz biofilma i potraže novi dom. Ovaj posljednji postupak poznat je kao "raspršivanje sjemena", prema Centru za biofilm inženjering.
Zašto formirati biofilm?
Za mikroorganizme življenje u sastavu biofilma ima određene prednosti. "Zajednice mikroba obično su otpornije na stres", rekao je Gerlach za Live Science. Potencijalni stresori uključuju nedostatak vode, visoki ili niski pH ili prisutnost tvari toksičnih za mikroorganizme, poput antibiotika, antimikrobnih lijekova ili teških metala.
Mnogo je mogućih objašnjenja za tvrdoću biofilma. Na primjer, tanak EPS pokrov može djelovati kao zaštitna barijera. Može pomoći u sprečavanju dehidracije ili djeluje kao štit protiv ultraljubičastog (UV) svjetla. Također, štetne tvari poput antimikrobnih lijekova, izbjeljivača ili metala ili se vežu ili neutraliziraju kada dođu u kontakt s EPS-om. Stoga se razrjeđuju u koncentracijama koje nisu smrtonosne prije nego što mogu dospjeti u različite stanice duboko u biofilmu, prema članku iz Nature Nature Microbiology iz 2004. godine.
Ipak, moguće je da određeni antibiotici prodiru u EPS i prođu kroz slojeve biofilma. Ovdje se može igrati još jedan zaštitni mehanizam: prisutnost bakterija koje fiziološki uspavaju. Da bi uspjeli, svi antibiotici zahtijevaju određenu razinu stanične aktivnosti. Dakle, ako su bakterije fiziološki uspavane za početak, nema mnogo toga da se antibiotik poremeti.
Drugi način zaštite od antibiotika je prisutnost posebnih bakterijskih stanica poznatih kao "perzistira". Takve se bakterije ne dijele i otporne su na mnoge antibiotike. Prema članku iz 2010. objavljenom u časopisu Cold Spring Harbor Perspectives in Biology, "ustraje" funkcija stvaranjem tvari koje blokiraju ciljeve antibiotika.
Općenito, mikroorganizmi koji žive zajedno kao biofilm imaju koristi od prisustva različitih članova zajednice. Gerlach je naveo primjer autotrofnih i heterotrofnih mikroorganizama koji zajedno žive u biofilmima. Autotrofi, poput fotosintetskih bakterija ili algi, mogu proizvesti vlastitu hranu u obliku organskog materijala (koji sadrži ugljik), dok heterotrofi ne mogu proizvesti vlastitu hranu i zahtijevaju vanjske izvore ugljika. "U tim zajednicama s više organizama često se križaju s hranom", rekao je.
Biofilmi i mi
S obzirom na ogroman raspon okruženja u kojima se susrećemo s biofilmima, ne čudi da oni utječu na mnoge aspekte ljudskog života. Ispod je nekoliko primjera.

Zdravlje i bolest
Kako su istraživanja napredovala tijekom godina, biofilmi - bakterijski i gljivični - uključeni su u različita zdravstvena stanja. U pozivu za prijavu za dodelu iz 2002. godine, Nacionalni zavodi za zdravstvo (NIH) primijetili su da biofilmi predstavljaju "preko 80 posto mikrobnih infekcija u tijelu".
Biofilmi mogu rasti na implantiranim medicinskim uređajima poput protetskih srčanih zalistaka, zglobne protetike, katetera i pejsmejkera. To zauzvrat dovodi do infekcije. Pojava je prvi put primijećena 1980-ih kada su bakterijski biofilmi pronađeni na intravenskim kateterima i pejsmejkerima. Za bakterijske biofilmove također se zna da uzrokuju zarazni endokarditis i upalu pluća kod cistične fibroze, prema članku Nature 2004. iz Microbiologije, među ostalim infekcijama.
"Razlog što je stvaranje biofilma veliki razlog za zabrinutost je taj što su unutar biofilma bakterije otpornije na antibiotike i druga važna dezinfekcijska sredstva koja biste mogli koristiti za kontrolu nad njima", rekao je AC Matin, profesor mikrobiologije i imunologije na Stanfordu Sveučilište. U stvari, u usporedbi sa slobodno plutajućim bakterijama, one koje rastu kao biofilm mogu biti i do 1.500 puta otpornije na antibiotike i druga biološka i kemijska sredstva, navodi se u članku Microbe-a. Matin je rezistentnost biofilma opisao u kombinaciji s općim povećanjem otpornosti na antibiotike među bakterijama kao "dvostruko veselje" i kao glavni izazov liječenju infekcija.
Gljivični biofilmi također mogu uzrokovati infekcije rastom na implantiranim uređajima. Vrste kvasca kao što su pripadnici roda Candida rastu na implantatima grudi, pejsmejkerima i protetskim srčanim zalistacima prema članku iz 2014. objavljenom u časopisu Cold Spring Harbor Perspectives in Medicine. Candida vrste rastu i na tkivima ljudskog tijela, što dovodi do bolesti poput vaginitisa (upala vagine) i orofaringealne kandidijaze (infekcije kvasca koja se razvija u ustima ili grlu). Međutim, autori primjećuju da rezistencija na lijekove nije prikazana u tim slučajevima.
Bioremedijacija
Ponekad su biofilmi korisni. "Bioremedijacija je općenito upotreba živih organizama ili njihovih proizvoda - na primjer enzima - za liječenje ili razgradnju štetnih spojeva", rekao je Gerlach. Napomenuo je da se biofilmi koriste u pročišćavanju otpadnih voda, onečišćenja teških metala poput kromata, eksploziva poput TNT-a i radioaktivnih tvari poput urana. "Mikrobi ih mogu ili degradirati, ili promijeniti njihovu pokretljivost ili otrovno stanje te ih zbog toga čine manje štetnima za okoliš i ljude", rekao je.
Nitrifikacija biofilmima jedan je oblik obrade otpadnih voda. Tijekom nitrifikacije amonijak se putem oksidacije pretvara u nitrite i nitrate. To mogu učiniti autotrofne bakterije, koje rastu kao biofilmi na plastičnim površinama, prema članku iz 2013. objavljenom u časopisu Water Research. Te su plastične površine veličine samo nekoliko centimetara i raspoređene su kroz vodu.
Eksplozivni TNT (2,4,6-trinitrotoluen) smatra se zagađivačem tla, površinskih i podzemnih voda. Kemijska struktura TNT-a sastoji se od benzena (šesterokutni aromatični prsten izrađen od šest atoma ugljika) vezanom u tri nitro skupine (NO2) i jedna metilna skupina (CH3). Mikroorganizmi razgrađuju TNT redukcijom, navodi se u članku iz 2007. objavljenom u časopisu Applied and Environmental Microbiology. Većina mikroorganizama smanjuje tri nitro skupine, dok neki napadaju aromatični prsten. Istraživači - Ayrat Ziganshin, Robin Gerlach i njegovi kolege - otkrili su da kvasac ima soj Yarrowia lipolytica bio je u stanju razgraditi TNT obje metode, iako prvenstveno napadom aromatičnog prstena.
Mikrobne gorivne ćelije
Mikrobne gorivne ćelije koriste bakterije za pretvaranje organskog otpada u električnu energiju. Mikrobi žive na površini elektrode i na nju prenose elektrone, što u konačnici stvara struju, rekao je Gerlach. Članak iz 2011. objavljen u internetskom časopisu Sveučilišta Južna Kalifornija u Illumin, primjećuje da bakterije koje napajaju mikrobne gorivne ćelije razgrađuju hranu i tjelesni otpad. To osigurava jeftin izvor energije i čistu održivu energiju.
U tijeku je istraživanje
Naš svijet zasićen je biofilmima. U stvari, do sredine 20. stoljeća na unutrašnjim površinama spremnika u kojima se nalaze bakterijske kulture pronađeno je više bakterija, nego što slobodno pluta u samoj tekućoj kulturi, prema članku iz Nature Nature Microbiology iz 2004. godine. Razumijevanje ovih složenih mikrobnih struktura aktivno je područje istraživanja.
"Biofilmi su nevjerojatne zajednice. Neki su ih uspoređivali s višećelijskim organizmima jer postoji puno interakcija između pojedinih stanica", rekao je Gerlach. "Nastavljamo učiti o njima i nastavljamo učiti o tome kako ih bolje kontrolirati; kako za smanjenu štetu, tako i za medicinu, ili za veću korist kao za bioremedijaciju. Neće nam nedostajati zanimljiva pitanja u tom području. "